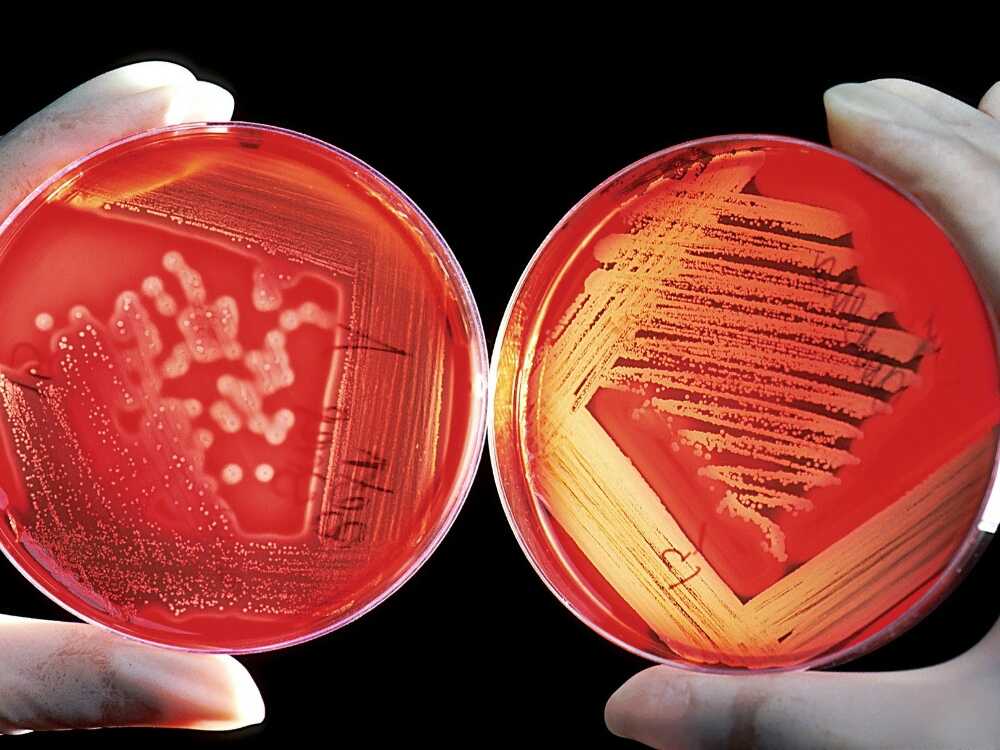
Para comprender la gravedad de la resistencia a los antimicrobianos, debemos abordar las razones de su dramático aumento y las consecuencias a las que nos enfrentamos.
La Organización Mundial de la Salud (OMS) ha calificado la resistencia a los antibióticos (RA) como una crisis de salud pública internacional en el siglo XXI, basándose en las estimaciones de los estudios de vigilancia disponibles. La carga real de la RA es difícil de cuantificar en algunas regiones del mundo debido a la falta de personal, equipo y recursos financieros. Dicho esto, sobre la base de los datos actuales, se prevé que la RA cause millones de muertes prematuras para 2050, con una pérdida acumulada para la economía mundial de billones de dólares.
Reseña histórica
El descubrimiento fortuito de la penicilina por Fleming en 1928 anunció la era de los antibióticos que revolucionó la medicina y salvó innumerables vidas. Una vez que los médicos vieron la eficacia de estos medicamentos llamados "bala mágica" en sus pacientes, comenzaron a recetar antibióticos no sólo para infecciones bacterianas, sino también para dolencias menores e infecciones virales.
Lamentablemente, el tratamiento exitoso con el antibiótico penicilina B-lactámico duró poco debido a la propagación de una enzima penicilinasa mediada por el plásmido en el Staphylococcus aureus. Aunque la resistencia a la penicilina estimuló las iniciativas para desarrollar nuevos medicamentos de B-lactam, nuevas clases de antibióticos naturales y antimicrobianos semisintéticos durante la llamada "era de oro" entre 1960 y 2000, también se produjo resistencia a estos antibióticos.
Esto no es una sorpresa, ya que los antibióticos y los genes AR han existido durante miles de años a medida que los microbios evolucionaban. Los arqueólogos han encontrado rastros del antibiótico tetraciclina en los huesos de los antiguos esqueletos nubios sudaneses desde el año 350-550 d.C.
Muchas bacterias susceptibles están expuestas a los antibióticos que son producidos naturalmente por otras bacterias y hongos. Como parte de la evolución, estas bacterias susceptibles desarrollan mecanismos de resistencia basados en la actividad de los genes de resistencia que superan la acción de los antibióticos. Se ha descubierto que los genes de resistencia están muy extendidos en el medio ambiente, verificando el origen de estos genes en depósitos de bacterias del suelo que son intrínsecamente resistentes a los antibióticos, es decir, resistencias ambientales.
En 2012, se aislaron bacterias con resistencia múltiple a los medicamentos (MDR) en la Cueva de Lechuguilla, un ecosistema subterráneo dentro del Parque Nacional de la Caverna de Carlsbad en Nuevo México (un sitio de Patrimonio Mundial de la UNESCO) que data de al menos cuatro millones de años atrás. En uno de estos aislamientos, se encontró que Paenibacillus era resistente a 18 antibióticos de uso frecuente como último recurso para tratar los superbichos, mucho antes de que los antibióticos se utilizaran para uso humano, animal y agrícola. Aunque este descubrimiento sugiere que el uso excesivo y el mal uso de los antibióticos por parte de los humanos no son los únicos responsables del surgimiento de la RA, sin duda contribuyen de manera significativa a la pandemia de resistencia a los antimicrobianos.
Las prácticas actuales, responsables del aumento de la biocarga de la resistencia a los antibióticos
El uso excesivo y el mal uso de los antibióticos para el consumo humano y animal, las prácticas deficientes de prevención y control de infecciones, la eliminación de desechos en gran escala por parte de los productos farmacéuticos y el depósito de aguas residuales de genes y organismos de resistencia contribuyen a la biocarga.
En una encuesta de prevalencia puntual sobre las infecciones asociadas a la atención sanitaria en Europa, 35? los pacientes hospitalizados en 2011 recibían antibióticos y, según un estudio realizado en los Estados Unidos en hospitales de cuidados agudos, una media del 59.3? todos los pacientes recibieron al menos una dosis de un agente antimicrobiano durante su estancia en el hospital.
En los países prósperos, las prescripciones excesivas e innecesarias se producían en la comunidad, mientras que en los países en desarrollo el uso excesivo se debía a los medicamentos de venta libre y a sistemas de reglamentación poco estrictos. En los entornos hospitalarios, el uso intenso y prolongado de drogas es probablemente el principal contribuyente a la aparición y propagación de infecciones adquiridas en la atención sanitaria por RA, mientras que en la comunidad, el hecho de no completar los suministros de antibióticos prescritos y la automedicación parecen contribuir a la RA.
Se ha informado de que más de 50? los antibióticos se producen en los animales destinados a la producción de alimentos y en la acuicultura para la promoción del crecimiento y el tratamiento de enfermedades. Aunque esta práctica está prohibida en Europa desde 2006, algunos países la mantienen.
Mecanismos de resistencia a los antibióticos
El mal uso y el uso excesivo de los antibióticos acelera la presión selectiva para la transferencia de las bacterias portadoras de genes de resistencia a las bacterias susceptibles, a través de elementos genéticos móviles llamados plásmidos, transposones e integrones.
La expresión de estos genes puede 1) afectar la permeabilidad de la pared celular que previene la penetración de los antibióticos en las bacterias, 2) modificar los canales de porina de las proteínas que restringen la entrada de los antibióticos en las bacterias, 3) crear bombas de efluentes que mueven los antibióticos fuera de las células bacterianas, 4) modificar los sitios de unión de los antibióticos en las bacterias, 5) desarrollar vías metabólicas alternativas, y 6) producir enzimas como las B-lactamasas que degradan o modifican los antibióticos.
Hasta la fecha, hay más de mil tipos ee B-lactamasas diferentes. Los genes que codifican las B-lactamasas se denominan bla seguidos del nombre de la enzima específica (por ejemplo, blaKPC). Varias bacterias Gram-negativas portadoras de genes de resistencia que expresan una o más B-lactamasas, son una importante amenaza clínica debido a su multirresistencia a las drogas y a su rápida propagación global. Para agravar el problema, más de un mecanismo de resistencia puede ser responsable de la resistencia a los antibióticos en estos organismos.
En 2008, se propuso el acrónimo "ESKAPE" patógenos (Enterococcus, Staphylococcus aureus, Klebsiella pneumoniae, Acinetobacter baumannii, Pseudomonas aeruginosa, Enterobacter spp o Escherichia coli) para destacar aquellos patógenos que a menudo escapan a los efectos de los antibióticos. Varios de estos organismos figuran en la lista de la OMS y los CDC de amenazas mundiales críticas de resistencia a los antimicrobianos. Estos organismos son cada vez más resistentes a los medicamentos (MDR), extensamente resistentes a los medicamentos (XDR) o pan-resistentes a los medicamentos (PDR).
Organismos multirresistentes de interés mundial
Se examinarán brevemente tres de los patógenos de ESKAPE, a saber, S. aureus, K. pneumoniae y A. baumannii, que muestran resistencia debido al meca y al blaNDM, respectivamente, así como dos patógenos emergentes, el mcr-1 en E. coli y la levadura, Candida.auris. En el decenio de 1960 surgieron las primeras cepas de S. aureus resistente a la meticilina (SARM) y ahora son una causa común tanto de la IAH como de las infecciones adquiridas en la comunidad (IAC).
Se estima que en 2011, sólo en los Estados Unidos, el SARM causó más de 80.000 infecciones invasivas, de las cuales sólo 14.000 ocurrieron en el hospital. En Europa, varios países implementaron planes de acción nacionales para reducir la propagación del SARM en las instalaciones de atención médica. Sobre la base de los datos generados por la Red Europea de Vigilancia de la Resistencia Antimicrobiana entre 2015 y 2018, muchos países comunicaron una disminución significativa del SARM, aunque a nivel mundial, el SARM sigue siendo un patógeno grave y de alta prioridad.
La Klebsiella pneumoniae, una bacteria intestinal común que puede causar infecciones mortales como la neumonía y la septicemia, es motivo de preocupación a nivel mundial. La resistencia mediada por las betalactamasas de espectro extendido (BLEE) afecta a todas las penicilinas, las cefalosporinas, incluidas las de tercera generación, y el aztreonam.
La prevalencia de las ESBL entre las cepas clínicas varía de un país a otro y entre las instituciones, y oscila entre
Desde entonces, la K. pneumoniae resistente al carbapenem (CR) surgió rápidamente como la causa más común de infecciones por carbapenem y multirresistentes a las drogas en las Enterobacteriaceae (CRE) y otros organismos en todo el mundo. Esto puede atribuirse en parte a los viajes internacionales, a la transmisión de paciente a paciente y a la transferencia horizontal entre especies de genes resistentes al KPC.
La colonización de CRE en el tracto gastrointestinal es importante como reservorio para la diseminación en instalaciones de atención médica y puede preceder a la infección. Los antibióticos múltiples o el tratamiento a largo plazo son factores de riesgo para el CRE. Un historial conocido de transporte de CRE en los últimos 12 meses antes de la hospitalización y la vinculación epidemiológica con una persona que se sabe que es un portador debe dar lugar a un aislamiento preventivo, una detección activa y precauciones de contacto.
En 2008, se detectó un nuevo gen blaNDM que codificaba para una metalo-B-lactamasa dependiente del zinc en un paciente sueco infectado con un organismo K. pneumoniae resistente al carbapenem y a múltiples fármacos.
Se pensó que había adquirido la infección en la India, aunque no se ha confirmado el origen exacto de este gen de resistencia a la metallo-B-lactamasa mediada por plásmidos en Nueva Delhi.
blaNDM se ha propagado a nivel mundial mediante la transferencia horizontal de genes a otros organismos Gram-negativos, incluidos otros organismos ESKAPE como A. baumannii y E. coli, impartiendo resistencia en estos organismos a la mayoría de los antibióticos excepto la tigeciclina y la colistina.
Sólo quedan unas pocas opciones terapéuticas para el tratamiento de las infecciones debidas a organismos resistentes a la carbapenema, una de ellas es un antiguo y bastante tóxico antibiótico, la colistina. El control de las infecciones y las intervenciones dirigidas a prevenir la diseminación de estos patógenos casi intratables son muy necesarios.
Desde finales del decenio de 1980, el A. baumannii resistente al carbapenem (CR), ha adquirido una prevalencia cada vez mayor en todo el mundo y causa importantes IAH, lo que suscita graves preocupaciones acerca de las opciones de tratamiento con antibióticos que quedan y que son sumamente limitadas. La resistencia al carbapenem puede ser el resultado de la sobreexpresión de OXA, IMP, VIM, SIM o, más recientemente, de carbapenemasas del tipo de la Metallo-Beta-Lactamasa (NDM) de Nueva Delhi.
En la actualidad, la A. baumannii resistente al carbapenem parece ser sólo susceptible a la colistina y la tigeciclina, aunque los datos que apoyan la eficacia de esos regímenes de tigeciclina son limitados. Se cree que las cepas resistentes a la colistina, que están aumentando en todo el mundo, están mediadas por la modificación de la membrana celular bacteriana, lo que da lugar a una interferencia en la capacidad del medicamento para unirse a los objetivos bacterianos.
La colistina también se ha utilizado como antibiótico de último recurso para las infecciones mortales en humanos causadas por numerosos miembros MDR de la familia Enterobacteriaceae.
Desde el descubrimiento en 2015 de la resistencia mediada por plásmidos en E. coli debido a un gen de resistencia a la colistina movilizado (mcr-1) en un cerdo en China, se han detectado genes mcr en múltiples miembros de la familia Enterobacteriaceae, incluida K. pneumoniae.
La colistina se ha utilizado en todo el mundo para la profilaxis o el tratamiento en medicina veterinaria para el manejo de afecciones respiratorias, y como promotores del crecimiento en rebaños de ganado en varios países. Hasta la fecha, se conocen al menos nueve genes mcr de resistencia a la colistina con distribución mundial, principalmente en muestras animales y ambientales y, en menor medida, en muestras clínicas humanas.
Aunque este artículo se ha centrado en la resistencia a los antibióticos, no hay que olvidar que la resistencia a múltiples fármacos también puede darse en los hongos. Candida auris es una especie emergente de levadura que se ha convertido en una grave amenaza para la salud mundial caracterizada por la colonización de la piel, la persistencia en los centros sanitarios y la resistencia a los antimicóticos.
- auris se describió por primera vez en 2009 a partir de un solo aislado, y desde entonces se ha notificado en más de 25 países de todo el mundo. La mayoría de las cepas enviadas a los CDC han sido resistentes al fluconazol, y hasta un tercio eran resistentes a la anfotericina B, considerada normalmente un tratamiento de último recurso.
Aunque la mayoría de las cepas de C. auris son susceptibles a las equinocandinas, puede desarrollarse resistencia mientras los pacientes están en tratamiento. Los mecanismos de la resistencia a los medicamentos antimicóticos de Candida auris no se comprenden bien, pero pueden deberse a mutaciones del ergosterol o a una bomba de efluvios. C. auris es también un importante problema de salud pública porque es difícil de identificar con los métodos de laboratorio habituales que pueden conducir a un tratamiento incorrecto, y se propaga fácilmente en los hospitales y los centros de atención a largo plazo.
Enfoques para abordar la resistencia antimicrobiana mundial
¿Nos dirigimos a una era post-antibiótica? En los últimos dos o tres decenios, no sólo nos hemos enfrentado a un aumento de microorganismos multirresistentes a los medicamentos (MDRO) que causan infecciones graves y a veces mortales, sino también a una disminución significativa del número de nuevos agentes antimicrobianos para tratar esas infecciones.
Afortunadamente, desde 2014 se han aprobado varios antibióticos nuevos, la mayoría de las modificaciones de las clases de antibióticos conocidas, debido a las iniciativas establecidas por un plan de acción mundial.
En resumen, la resistencia a los antimicrobianos es un problema mundial que no puede ignorarse. Para comprender la gravedad de la resistencia a los antimicrobianos, es necesario abordar las razones del drástico aumento de la resistencia a los antimicrobianos y las consecuencias a las que nos enfrentamos, así como las posibles soluciones al problema.
En mayo de 2015, la Asamblea Mundial de la Salud aprobó un plan de acción mundial y un enfoque de "Una salud" para promover las mejores prácticas mediante la mejora de la prevención y el control de las infecciones, la prevención de la aparición y la propagación de la resistencia a los antibióticos mediante el uso óptimo de los mismos en los seres humanos y los animales, la inversión en la investigación y el desarrollo de nuevos antimicrobianos, clases de medicamentos y vacunas, la desvinculación de los pagos por antibióticos del volumen utilizado y, si no se cumplen, la aplicación de una política de pago o de juego que exija a las empresas farmacéuticas pagar un cargo si no tienen un programa activo de investigación y desarrollo de antibióticos, y la inversión en la investigación y el desarrollo de herramientas de laboratorio de diagnóstico, por ejemplo, herramientas de punto de atención rápida, para el manejo óptimo de los pacientes.
No olvides ser parte de nuestro siguiente webinar, en el cuál tocaremos temas importantes de la industria de la salud.
Regístrate sin costo aquí: Webinar Conexión Expo Med